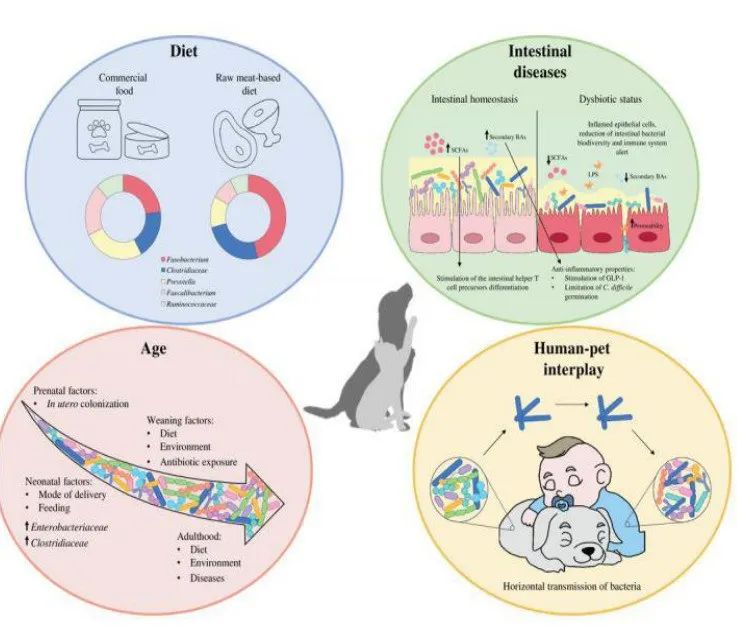
肠道微生物除了通过降解其他不可消化的膳食化合物以及产生各种短链脂肪酸,为结肠细胞提供营养的代谢物来为宿主提供营养支持的代谢作用之外,人们相信肠道微生物群还与宿主的免疫系统存在一定联系。
已有研究证明,微生物生态系统的平衡涉及多种生理和代谢功能。值得注意的是,肠道微生物群落调节局部和全身免疫反应,促进肠道屏障完整性,影响肠道稳态和功能,并提供为肠道提供保护,减少肠道病原体定植。宿主的肠道微生物可通过代谢产物参与各种途径,从而影响机体的先天免疫系统。后者又可以由细菌产物(例如短链脂肪酸或维生素)以及宿主初级代谢物,这些初级代谢物可以通过肠道菌群产生的酶促转化为次级代谢物。
同时,为了确保肠道稳态,胃肠黏膜一方面作为营养吸收和免疫感应的半透屏障,另一方面防止潜在有害微生物、化合物和抗原通过。然而,当肠上皮屏障发生功能或生理损伤时,肠通透性改变等异常后果可能会影响肠内稳态。类似地,肠道微生物群的丰度或组成的改变以及其功能活动的剧烈变化可能导致适应性免疫反应的失调,并激活炎症过程,这反过来可能与感染易感性增加有关。这些肠道扰动中的一种或多种通常与不同疾病的发作有关,例如慢性肠病(CE)、急性出血性或非出血性腹泻综合征,甚至是犬猫的肠癌。
尤其值得注意的是,由于炎症相关的肠道屏障通透性增强,肠腔中生物可利用氧的增加似乎在改变肠道微生物群组成有利于兼性厌氧菌增殖中发挥核心作用,尤其是肠杆菌科的成员(Vazquez-Baeza et al 2016)。
然而,尽管在该领域进行了大量研究,但尚不清楚肠道中发生的功能和微生物分类学变化是否是炎症性肠病的原因或影响。这对狗和猫来说更加困难,因为在大多数情况下,炎症性肠病的诊断是在抗生素治疗无反应后确定的,这本身就会改变微生物群的组成。
肠道微生物群失调会导致宠物多种胃肠道疾病产生,主要是以下几种:
狗和猫的主要急性肠道疾病是急性单纯性腹泻(AD)和急性出血性腹泻综合征(AHDS)。这两种肠道疾病的临床结果不同。急性单纯性腹泻(AD)的临床特征是轻微腹泻,但急性出血性腹泻综合征(AHDS)的临床后果更为严重,包括与肠黏膜出血性病变相关的出血性腹泻、脱水、嗜睡和厌食。尽管这两种疾病在组织学和症状上存在差异,但AD和AHDS在肠道微生物组成方面表现出相似的变化。在这种情况下,对受AD或AHDS影响的狗进行的一项研究观察到,与健康对照组相比,Blautia、Faecalibacterium、 Ruminococcus和Turicibacter属的相对丰度显着降低,而梭菌属相对丰度升高。
另一项研究显示,AD或AHDS相关犬类粪便样本中的梭菌属丰度显着增加,尤其是产气荚膜梭菌,同时普氏菌属、布劳氏菌属、粪杆菌属、毛螺菌科和瘤胃球菌科的数量减少,在AD和AHDS疾病中均观察到此现象。尽管这些物种是健康犬猫胃肠道的肠道共生菌,但梭状芽胞杆菌在AHDS中的病理作用最近得到证实,在患有AHDS的狗的内镜活检组织的坏死黏膜表面发现了梭状芽孢杆菌样细菌并伴有异常增殖产气荚膜梭菌。进一步的研究确定了netF阳性A型产气荚膜梭菌细菌是造成AHDS典型肠道损伤的原因。
产气荚膜梭菌在患有AD的猫中没有显示出统计学上显着的相对丰度增加,表明该物种在猫胃肠道疾病中没有发挥重要作用。取而代之的是,大肠杆菌在患有AD的猫中显示出统计学上显着的相对丰度增加,并且涉及其他胃肠道疾病。然而,需要进一步的研究来评估大肠杆菌作为菌群失调导致猫肠道疾病的肠道病原体的确切作用。应该指出的是,某些其他分类群,例如Faecalibacterium和 Roseburia,被证明会导致患有AD的猫的粪便样本中的相对丰度降低。
慢性肠病(CE)是指一组异质性肠道疾病,通常根据其对治疗的反应进行分类,包括饮食反应性肠病(FRE)、抗生素反应性肠病(ARE)和免疫抑制剂反应性肠病(IRE)和特发性炎症性肠病(IBD)。尽管有不同的病因,但狗和猫的CE疾病的特点是持续性和复发性临床症状的重叠,包括肠道炎症的血液证据以及呕吐、腹泻、缺食、腹痛和体重减轻。尽管肠道微生物群参与CE的病因学已被广泛接受,但由于缺乏研究肠道微生物的标准方案,仍难以确定与这些肠道疾病直接相关的特定微生物生物标志。
但是,研究已经确定了一些共同特征。在患有CE的狗中,梭杆菌的相对丰度以及拟杆菌门的一些代表,即拟杆菌科与健康对照组相比减少。类似地,在患有CE的狗中,厚壁菌门的几个成员的相对丰度下降,包括巨单胞菌属、瘤胃球菌属、粪杆菌属、布劳氏菌属和Turicibacter以及毛螺菌科。相反,变形杆菌门的某些成员,特别是肠杆菌科的某些成员,包括特别是大肠杆菌,在患有CE的狗中显示出显着的相对丰度增加。
根据在狗身上观察到的情况,一项涉及16SrRNA微生物分析的研究表明,与健康对照组相比,患有CE的猫中属于瘤胃球菌科和Turicibacter属的细菌分类群数量明显少于健康对照组。同样,一些拟杆菌属成员,尤其是与人类炎症性肠病缓解有关的拟杆菌属放线菌门在CE情况下显示出丰度下降的趋势。此外,采用不同实验方法(包括16S rRNA测序和荧光原位杂交)的各种研究表明,患有CE的猫通常表现出双歧杆菌属的相对丰度下降,而这种趋势尚未在患有CE的狗身上发现。
猫和狗的便秘患病率没有得到很好的统计和报道,宠物主人很难量化排便频率和确认宠物是否发生便秘。尽管如此,便秘可能是宠物中相对常见的临床问题,尤其是猫中,便秘的现象更加严重(Chandler 2013)。
现有研究尚未确定宠物便秘与胃肠道微生物组组成之间的明确联系,包括特定细菌群的丰度的改变是否能引发便秘。尽管如此,已有关于人类肠道菌群研究证据表明,便秘与胃肠道微生物组组成之间存在密切联系。
对宠物胃肠道微生物组与便秘之间的机制关系的研究甚至更少,特定细菌类群对胃肠道运动的影响机制并不明确。一项体外研究表明,梭菌、乳杆菌、脱硫弧菌和甲基杆菌的丰度降低可能通过影响血清素受体来影响胃肠道运动,从而导致慢性便秘的发展。肠道细菌产生的短链脂肪酸,如乙酸盐和丁酸盐,也被认为是改变血清素可用性的一种手段,从而影响肠道的运动和分泌。一项针对便秘猫的干预试验评估了含有多种菌株的益生菌 (SLAB51),包括:嗜热链球菌DSM32245;嗜酸乳杆菌DSM32241;植物乳杆菌DSM32244;干酪乳杆菌DSM32243;瑞士乳杆菌DSM322422;短乳杆菌DSM27961;乳双歧杆菌DSM32246和乳双歧杆菌DSM32247。实验结果显示,粪便评分和粘膜组织学有所改善。治疗后,链球菌和乳杆菌的数量显着增加,双歧杆菌和拟杆菌的数量呈增加趋势。
尽管关于猫和狗的数据有限,但一些综述总结了益生菌对人类便秘有益影响的研究。这些研究支持使用益生菌治疗便秘、减少胃肠道转运时间、增加大便频率、改善大便稠度和改善胃肠道症状。益生菌对人类便秘的影响潜在机制集中在肠腔环境、免疫系统、肠神经系统和中枢神经系统之间的相互作用,这些因素高度相关并影响肠道运动。
宠物肥胖是一个严重的问题。根据宠物肥胖预防协会最近的一份报告,美国60%的猫和56%的狗被归类为超重或肥胖。肥胖还与多种其他疾病相关,例如糖尿病(DM)、骨关节炎、心血管疾病、皮肤病和寿命缩短。研究者认为主要有以下几个因素会使动物易患肥胖,包括胃肠道微生物组、遗传、绝育、活动水平降低以及高脂肪和高能量饮食。
一些报告发现,肥胖和正常体型猫和狗的胃肠道微生物组的组成不同。具体而言,与正常体型狗相比,放线菌门和 Roseburia属的细菌在肥胖狗中的数量明显更多。在猫中,与正常体型猫相比,肥胖和超重猫的梭状芽孢杆菌簇XIVa群、拟杆菌属和梭杆菌属的丰度较低,但属于肠杆菌科和肥胖和超重猫的梭菌簇IⅣ组较高。此外,多项研究发现,不同的饮食对肥胖动物和正常体型动物的胃肠道微生物群有不同的影响。
胃肠道微生物组通过对肠道的直接影响及其对其他器官的间接影响,从而影响宠物机体肥胖的发展和进程。肠道微生物群已被证明会影响胆汁酸的代谢;细菌代谢产生的游离胆汁酸可以抑制细菌种群的生长,例如乳酸杆菌和双歧杆菌,它们被认为可以预防肥胖。此外,肠道中的几种细菌(例如梭状芽孢杆菌、海莱蒙梭状芽孢杆菌和希拉尼梭状芽孢杆菌)含有与胆汁酸代谢有关的基因。
由于胆汁酸被认为有助于肠道激素分泌以及葡萄糖和脂质代谢,因此胃肠道微生物组对胆汁酸的影响也可能影响这些过程。胃肠道微生物组的破坏已被证明会抑制脂蛋白脂肪酶,这会导致脂肪组织和肝脏、胰腺和心脏中的甘油三酯过量沉积(陆淋丽等2021)。
肠道微生物组影响体重变化的机制尚不清楚。然而,据报道吲哚可以调节胰高血糖素样肽-1的分泌,从而刺激胰岛素分泌,并通过延迟胃排空、引起饱腹感和减少食物摄入来帮助减轻体重。同样,发现大肠杆菌分泌的蛋白质直接激活宿主饱腹感通路,刺激GLP-1释放,当这些蛋白质腹膜内给予大鼠时,与对照组相比,它们的食物摄入量减少。
来源:罗建《不同宠物用益生菌产品中乳酸菌的益生特性评价》